Nuove prospettive nella lotta contro malattie genetiche rare e disturbi neurodegenerativi emergono da uno studio condotto dal Consiglio Nazionale delle Ricerche (Cnr-Ibbc) e dall’Università di Napoli Federico II. I ricercatori hanno scoperto un ruolo inedito della proteina DDX11, fondamentale per la salute del DNA umano, che si rivela anche un attore cruciale nel processo di autofagia cellulare.
Pubblicata sulla rivista scientifica internazionale Autophagy, la ricerca è guidata da Francesca M. Pisani, dirigente di ricerca del Cnr-Ibbc, in collaborazione con Maurizio Renna del Dipartimento di Medicina Molecolare e Biotecnologie Mediche dell’Università Federico II. Lo studio è supportato dal progetto europeo CohesiNet e dal programma nazionale CNCCS-B (FOE – CNR) per la ricerca sulle malattie rare.
Cos’è DDX11 e perché è importante
La proteina DDX11 è una DNA elicasi, ovvero un enzima che srotola la doppia elica del DNA per consentire la replicazione e la riparazione del genoma. Mutazioni in DDX11 sono alla base della Warsaw Breakage Syndrome (WABS), una malattia genetica rara appartenente al gruppo delle coesinopatie, che colpisce lo sviluppo fisico e neurologico.
Precedenti ricerche del Cnr-Ibbc avevano già mostrato il coinvolgimento di DDX11 nel mantenimento della coesione dei cromatidi fratelli durante la divisione cellulare. Tuttavia, la nuova scoperta svela un ulteriore meccanismo d’azione nel citoplasma cellulare, dove DDX11 regola direttamente il processo di autofagia.
Autofagia e neuroprotezione: il nuovo ruolo di DDX11
L’autofagia è un processo biologico essenziale per il riciclo dei componenti cellulari danneggiati, come organelli e proteine non funzionanti. La proteina DDX11 si è rivelata indispensabile per la corretta formazione degli autofagosomi, le vescicole che trasportano i rifiuti cellulari verso i lisosomi per la loro degradazione.
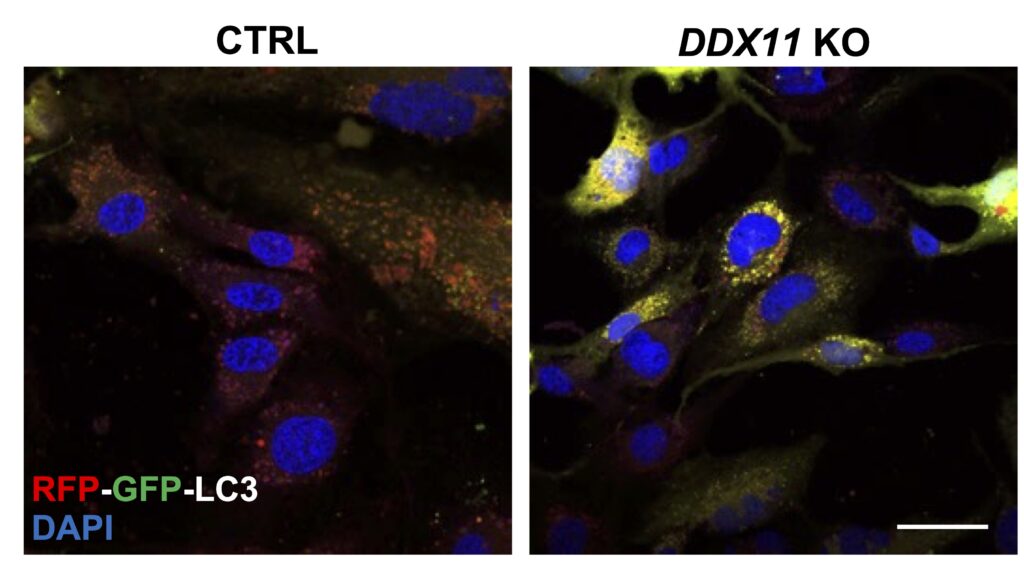
“In assenza di DDX11, le cellule non riescono a formare correttamente gli autofagosomi”, spiega Raffaella Bonavita, prima autrice dello studio. “Questo compromette l’eliminazione di aggregati tossici come quelli associati alla proteina huntingtin mutata, implicata nella Corea di Huntington.”
Un aspetto centrale emerso dallo studio è l’interazione tra DDX11 e p62/SQSTM1, un recettore cruciale per la selezione e il trasporto dei materiali danneggiati. Anche le cellule derivate da pazienti affetti da WABS mostrano un flusso autofagico alterato, suggerendo un legame diretto tra difetti dell’autofagia e patologie genetiche.
Implicazioni per Alzheimer, Parkinson e altre malattie neurodegenerative
L’autofagia è considerata una funzione chiave per la salute del sistema nervoso, e la sua alterazione è stata associata a patologie come il morbo di Alzheimer, il morbo di Parkinson, la SLA e l’atassia con aprassia oculomotoria di tipo 2 (AOA2).
“Comprendere come DDX11 regoli l’autofagia potrebbe rivelarsi decisivo non solo per chiarire le basi molecolari della WABS”, sottolinea Francesca M. Pisani, “ma anche per sviluppare nuove strategie terapeutiche per le malattie neurodegenerative”.
Ricerca italiana in prima linea per la medicina di precisione
Questo studio rafforza il ruolo della ricerca scientifica italiana nella scoperta di nuovi target molecolari e nella comprensione dei meccanismi cellulari alla base delle patologie complesse. Dalla genetica all’autofagia, DDX11 si conferma una proteina centrale nella medicina del futuro.